
- May -akda Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Huling binago 2025-01-22 17:12.
Yunit ng atomic mass . An yunit ng atomic mass (pinaikling: amu, u, o Da) ay a yunit ng pagsukat nakasanayan na yan sukatin ang misa ng mga atomo . Ang yunit ng atomic mass ay katumbas ng ?1⁄12 ng misa ng carbon-12. Ang salitang 'dalton' ay mas ginagamit sa paglipas ng panahon.
Sa ganitong paraan, paano sinusukat ang atomic mass?
Ang atomic mass ng isang elemento ay ang average misa ng mga atomo ng isang elemento sinusukat sa atomic mass unit (amu, kilala rin bilang daltons, D). Ang atomic mass ay isang weighted average ng lahat ng isotopes ng elementong iyon, kung saan ang misa ng bawat isotope ay pinarami ng kasaganaan ng partikular na isotope na iyon.
Higit pa rito, may mga yunit ba ang atomic mass? Habang atomic mass ay isang ganap misa , kamag-anak na isotopic misa ay isang walang sukat na numero na may no mga yunit . Halimbawa, ang kamag-anak na isotopic misa ng isang carbon-12 atom ay eksaktong 12. Para sa paghahambing, ang atomic mass ng isang carbon-12 atom ay eksaktong 12 daltons.
Kung isasaalang-alang ito, aling dami ang sinusukat sa atomic mass unit?
Mass ng atom . Mass ng atom , ang dami ng bagay na nakapaloob sa isang atom ng isang elemento. Ito ay ipinahayag bilang isang multiple ng one-twelfth ng misa ng carbon-12 atom , 1.992646547 × 10−23 gramo, na itinalaga ng isang atomic mass ng 12 mga yunit . Sa iskala na ito 1 yunit ng atomic mass (amu) ay tumutugma sa 1.660539040 × 10−24 gramo.
Ano ang atomic mass unit sa kimika?
Sa kimika , isang yunit ng atomic mass o AMU ay isang pisikal na pare-parehong katumbas ng isang-labindalawa ng misa ng isang hindi nakatali atom ng carbon-12. Ito ay isang yunit ng misa ginamit upang ipahayag atomic mass at molekular masa.
Inirerekumendang:
Paano mo kinakalkula ang average na atomic mass ng strontium?

Kaya, kinakalkula namin ito sa pamamagitan ng pagkuha ng timbang na masa ng bawat isa sa mga isotopes at pagdaragdag ng mga ito nang sama-sama. Kaya, para sa unang masa, magpaparami tayo ng 0.50% ng 84 (amu - atomic mass units) = 0.042 amu, at idagdag ito sa 9.9% ng 86 amu = 8.51 amu, at iba pa
Paano natutukoy ang average na atomic mass sa periodic table?

Ang average na atomic mass para sa isang elemento ay kinakalkula sa pamamagitan ng pagbubuod ng mga masa ng isotopes ng elemento, bawat isa ay pinarami ng natural na kasaganaan nito sa Earth. Kapag gumagawa ng anumang mga kalkulasyon ng masa na kinasasangkutan ng mga elemento o compound, palaging gumamit ng average na atomic mass, na makikita sa periodic table
Paano mo kinakalkula ang atomic mass ng boron?
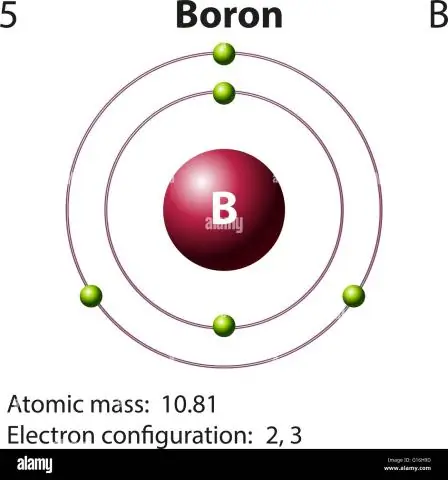
Para sa boron, magiging ganito ang equation na ito: 5 protons + 5 neutrons = 10 atomic mass units (AMU) o, para sa mas karaniwang nangyayaring boron isotope (approx. 5 protons + 6 neutrons = 11 AMU
Paano mo kinakalkula ang mga problema sa pagsasanay ng atomic mass?

VIDEO Pagkatapos, paano mo malulutas ang mga problema sa atomic mass? Upang kalkulahin ang atomic mass ng isang atom ng isang elemento, idagdag ang misa ng mga proton at neutron. Halimbawa: Hanapin ang atomic mass ng isang isotope ng carbon na mayroong 7 neutron.
Bakit ang periodic table ay nakaayos ayon sa atomic number at hindi atomic mass?

Bakit ang Periodic Table ay nakaayos ayon sa atomic number at hindi atomic mass? Ang atomic number ay ang bilang ng mga proton sa nucleus ng bawat atom ng elemento. Ang numerong iyon ay natatangi sa bawat elemento. Ang masa ng atom ay tinutukoy ng bilang ng mga proton at neutron na pinagsama
