
- May -akda Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Huling binago 2025-01-22 17:12.
VIDEO
Pagkatapos, paano mo malulutas ang mga problema sa atomic mass?
Upang kalkulahin ang atomic mass ng isang atom ng isang elemento, idagdag ang misa ng mga proton at neutron. Halimbawa: Hanapin ang atomic mass ng isang isotope ng carbon na mayroong 7 neutron. Makikita mo mula sa periodic table na ang carbon ay may isang atomic bilang ng 6, na siyang bilang ng mga proton.
Bukod pa rito, ano ang atomic mass number? Ang Pangkalahatang numero (simbolo A, mula sa salitang Aleman na Atomgewicht [ atomic timbang]), tinatawag din atomic mass number o nucleon numero , ay ang kabuuan numero ng mga proton at neutron (magkasamang kilala bilang mga nucleon) sa isang atomic nucleus. Ang Pangkalahatang numero ay naiiba para sa bawat magkakaibang isotope ng isang elemento ng kemikal.
Ang dapat ding malaman ay, ano ang formula ng atomic mass?
Katamtaman atomic mass = f1M1 + f2M2 +… + f M kung saan ang f ay ang fraction na kumakatawan sa natural na kasaganaan ng isotope at ang M ay ang misa bilang (bigat) ng isotope. Ang karaniwan atomic mass ng isang elemento ay matatagpuan sa periodic table, kadalasan sa ilalim ng elemental na simbolo.
Ano ang average na atomic mass sa kimika?
Ang average na atomic mass ng isang elemento ay ang kabuuan ng masa ng mga isotopes nito, bawat isa ay pinarami ng natural na kasaganaan nito (ang decimal na nauugnay sa porsyento ng mga atomo ng elementong iyon na nasa isang ibinigay na isotope).
Inirerekumendang:
Paano mo kinakalkula ang average na atomic mass ng strontium?

Kaya, kinakalkula namin ito sa pamamagitan ng pagkuha ng timbang na masa ng bawat isa sa mga isotopes at pagdaragdag ng mga ito nang sama-sama. Kaya, para sa unang masa, magpaparami tayo ng 0.50% ng 84 (amu - atomic mass units) = 0.042 amu, at idagdag ito sa 9.9% ng 86 amu = 8.51 amu, at iba pa
Paano mo kinakalkula ang atomic mass ng boron?
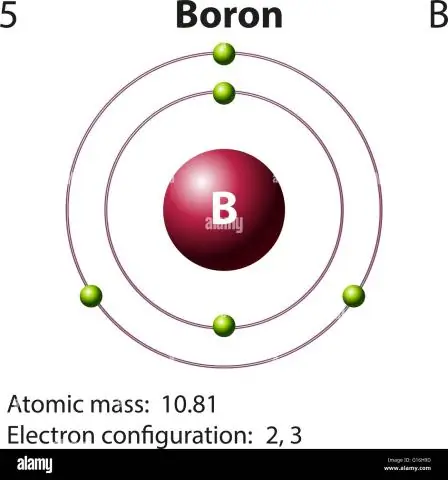
Para sa boron, magiging ganito ang equation na ito: 5 protons + 5 neutrons = 10 atomic mass units (AMU) o, para sa mas karaniwang nangyayaring boron isotope (approx. 5 protons + 6 neutrons = 11 AMU
Paano mo malulutas ang paglilimita sa mga problema sa masa ng reactant mass?

Hanapin ang naglilimitang reagent sa pamamagitan ng pagkalkula at paghahambing ng dami ng produkto na gagawin ng bawat reactant. Balansehin ang chemical equation para sa chemical reaction. I-convert ang ibinigay na impormasyon sa mga moles. Gumamit ng stoichiometry para sa bawat indibidwal na reactant upang mahanap ang masa ng produktong ginawa
Paano mo kinakalkula ang mga problema sa titration?

Problema sa Titration Step-by-Step na Solusyon Hakbang 1: Tukuyin ang [OH-] Bawat mole ng NaOH ay magkakaroon ng isang mole ng OH-. Hakbang 2: Tukuyin ang bilang ng mga moles ng OH- Molarity = bilang ng mga moles/volume. Hakbang 3: Tukuyin ang bilang ng mga moles ng H+ Hakbang 4: Tukuyin ang konsentrasyon ng HCl
Bakit ang periodic table ay nakaayos ayon sa atomic number at hindi atomic mass?

Bakit ang Periodic Table ay nakaayos ayon sa atomic number at hindi atomic mass? Ang atomic number ay ang bilang ng mga proton sa nucleus ng bawat atom ng elemento. Ang numerong iyon ay natatangi sa bawat elemento. Ang masa ng atom ay tinutukoy ng bilang ng mga proton at neutron na pinagsama
