
Talaan ng mga Nilalaman:
- May -akda Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Huling binago 2025-01-22 17:12.
Pinagmulan ang Henderson-Hasselbalch Equation
- Kunin ang reaksyon ng ionization ng mahinang acid (HA):
- Ang dissociation constant Ka ng reaksyon sa itaas ay magiging:
- Pagkatapos ay mula sa equation (2) ilabas ang [H?] sa kaliwang bahagi (solve para sa H?):
- Palitan ang pH at pKa sa equation (4):
Katulad nito, ano ang equation ng Henderson sa kimika?
Na-update noong Agosto 10, 2019. Ang Henderson Hasselbalch equation ay isang tinatayang equation na nagpapakita ng kaugnayan sa pagitan ng pH o pOH ng isang solusyon at ng pKa o pKb at ang ratio ng mga konsentrasyon ng dissociated kemikal uri ng hayop.
Gayundin, ano ang ibig sabihin ng pKa? Mga Pangunahing Takeaway: Kahulugan ng pKa Ang pKa ang halaga ay isang paraan na ginagamit upang ipahiwatig ang lakas ng isang acid. pKa ay ang negatibong log ng acid dissociation constant o halaga ng Ka. Isang mas mababa pKa ang halaga ay nagpapahiwatig ng mas malakas na acid. Iyon ay, ang mas mababang halaga ay nagpapahiwatig ng acid na mas ganap na naghihiwalay sa tubig.
Kung isasaalang-alang ito, ano ang pKa formula?
pKa ay tinukoy bilang -log10 Ka kung saan si Ka = [H+][A-] / [HA]. Mula sa mga ekspresyong ito posibleng makuha ang Henderson-Hasselbalch equation which is. pKa = pH + log [HA] / [A-] Sinasabi nito sa atin na kapag ang pH = pKa pagkatapos ay mag-log [HA] / [A-] = 0 samakatuwid [HA] = [A-] ibig sabihin, pantay na halaga ng dalawang anyo.
Ang tubig ba ay isang buffer?
Tubig ay isang buffer kahit mahirap. Ito ay dahil ang H20 ay nag-ionize upang bumuo ng H30+ at OH-. Upang bumuo ng isang acidic buffer buffer kailangan mo ng mahinang acid na may conjugate base. Dahil magkakaroon ng hydronium at hydroxide ions na naroroon oo ito ay gumaganap bilang a buffer ngunit ito ay isang kakila-kilabot.
Inirerekumendang:
Paano mo mapapatunayan ang batas ng malalaking numero?

VIDEO Alamin din, paano mo ipapaliwanag ang batas ng malalaking numero? Ang batas ng malalaking numero nagsasaad na ang isang naobserbahang sample average mula sa a malaki ang sample ay magiging malapit sa tunay na average ng populasyon at na ito ay lalapit kapag mas malaki ang sample.
Paano mo mapapatunayan na ang mga linya ay parallel sa mga patunay?

Ang una ay kung ang mga kaukulang anggulo, ang mga anggulo na nasa parehong sulok sa bawat intersection, ay pantay-pantay, kung gayon ang mga linya ay parallel. Ang pangalawa ay kung ang mga kahaliling panloob na anggulo, ang mga anggulo na nasa magkabilang panig ng transversal at sa loob ng magkatulad na mga linya, ay pantay, kung gayon ang mga linya ay parallel
Paano mo mapapatunayan ang pagpapatuloy?

Depinisyon: Ang isang function na f ay tuloy-tuloy sa x0 sa domain nito kung para sa bawat ϵ > 0 ay mayroong δ > 0 na kapag ang x ay nasa domain ng f at |x − x0| < δ, mayroon kaming |f(x) − f(x0)| < ϵ. Muli, sinasabi natin ang f ay tuloy-tuloy kung ito ay tuloy-tuloy sa bawat punto sa domain nito
Paano mo mapapatunayan na ang kasalukuyang nagdadala ng konduktor ay gumagawa ng magnetic field?

Ang anumang kasalukuyang nagdadala ng conductor ay gumagawa ng amagnetic field na nagpapalipat-lipat sa sarili nito ayon sa bersyon ng grip ng Right-hand rule (kung ang conventionalcurrent ay nasa direksyon ng hinlalaki, ang mga daliri ay kumukulot sa direksyon ng magnetic field)
Paano mo mapapatunayan ang 2 tatsulok na magkatulad gamit ang side angle side SAS similarity postulate?
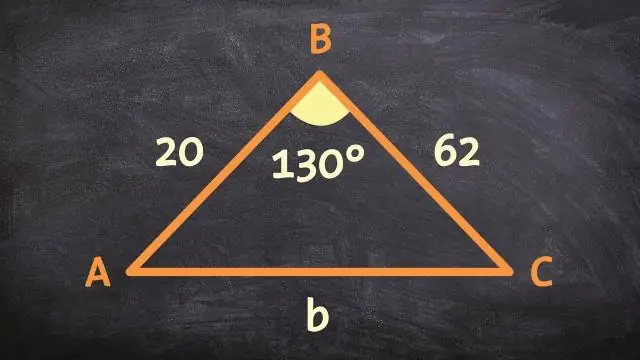
Ang SAS Similarity Theorem ay nagsasaad na kung ang dalawang panig sa isang tatsulok ay proporsyonal sa dalawang panig sa isa pang tatsulok at ang kasamang anggulo sa pareho ay magkapareho, kung gayon ang dalawang tatsulok ay magkatulad. Ang pagbabagong pagkakatulad ay isa o higit pang mahigpit na pagbabagong sinusundan ng dilation
