
Talaan ng mga Nilalaman:
- May -akda Miles Stephen stephen@answers-science.com.
- Public 2024-01-18 08:19.
- Huling binago 2025-01-22 17:12.
Heat of Solution o Enthalpy of Solution Chemistry Tutorial
- Kinakalkula ang dami ng enerhiya na inilabas o hinihigop. q = m × Cg × ΔT. q = dami ng enerhiya na inilabas o hinihigop.
- kalkulahin mga nunal ng solute. n = m ÷ M. n = mga moles ng solute.
- Dami ng enerhiya ( init ) na inilabas o hinihigop sa bawat mole ng solute ay kinakalkula. ΔHsoln = q ÷ n.
Kaya lang, paano mo kinakalkula ang init ng solusyon sa kJ mol?
Halimbawa ng Enthalpy of Solution (Heat of Solution)
- Kalkulahin ang inilabas na init, q, sa joules (J), sa pamamagitan ng reaksyon: q = masa(tubig) × tiyak na kapasidad ng init(tubig) × pagbabago sa temperatura(solusyon)
- Kalkulahin ang mga moles ng solute (NaOH(s)): moles = masa ÷ molar mass.
- Kalkulahin ang pagbabago ng enthalpy, ΔH, sa kJ mol-1 ng solute:
ano ang init ng solusyon ng NaOH? Ang tinatanggap na halaga para sa init ng solusyon ng NaOH ay 44.2 kJ/mol at para sa NH4NO3, ito ay 25.4 kJ/mol.
Kasunod nito, maaari ring magtanong, paano mo kinakalkula ang init na hinihigop?
Ang hinihigop ng init ay kalkulado sa pamamagitan ng pagpaparami ng mga moles ng tubig sa molar init ng singaw. 5. Ang singaw ay pinainit mula 100oC hanggang 140oC. Ang hinihigop ng init ay kalkulado sa pamamagitan ng paggamit ng tiyak init ng singaw at ang equation ΔH=cp×m×ΔT.
Ano ang tiyak na init ng NaOH?
Pinakamababang Temperatura bilang Paunang Temperatura=43.5°C. Densidad ng HCl & NaOH Soultion=1.04 g/mL. Tukoy na init ng HCl & NaOH Solusyon=4.017 J/g°C.
Inirerekumendang:
Paano mo kinakalkula ang enerhiya ng init sa pamamagitan ng tubig?

Pagkalkula ng Inilabas na Init Susunod, gagamitin mo ang Q = mc ∆T, ibig sabihin, Q = (100 + 100) x4.18 x 8. Hinahati ang tiyak na kapasidad ng init ng tubig, 4181 joules/kg degrees Celsius sa 1000 upang makuha ang figure para sa joules/g degrees C. Ang sagot ay 6,688, ibig sabihin ay 6688 joules ng init ang inilabas
Paano natin kinakalkula ang tiyak na kapasidad ng init?
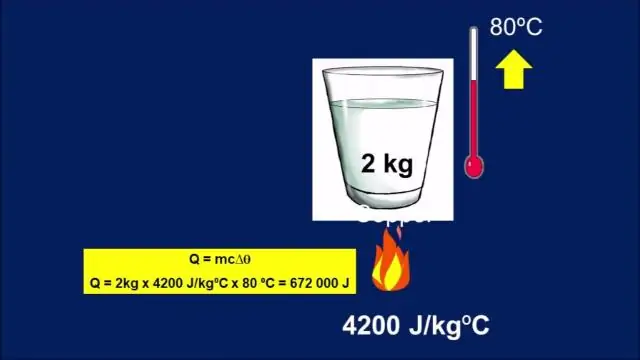
Ang mga yunit ng tiyak na kapasidad ng init ay J/(kg °C) o katumbas ng J/(kg K). Ang kapasidad ng init at ang tiyak na init ay nauugnay sa pamamagitan ng C=cm o c=C/m. Ang mass m, tiyak na init c, pagbabago sa temperatura ΔT, at init na idinagdag (o ibinawas) Q ay nauugnay sa pamamagitan ng equation: Q=mcΔT
Ano ang pagkakaiba sa pagitan ng hydration energy at solvation energy?

Solvation, ay ang proseso ng pagkahumaling at pag-uugnay ng mga molekula ng isang solvent sa mga molekula o mga ion ng asolute. Habang natutunaw ang mga ion sa isang solvent ay kumakalat sila at napapalibutan ng mga solvent na molekula. Ang hydration ay ang proseso ng pagkahumaling at pag-uugnay ng mga molekula ng tubig sa mga molekula o ion ng isang solute
Ang solvation ba ay isang kemikal na reaksyon?

Ayon sa UPAC 'ang solvation ay isang pakikipag-ugnayan ng isang solute sa solvent, na humahantong sa stabilization ng solute species sa solusyon.' Sa buod, ang solvation ay hindi kemikal na reaksyon, at nagpatuloy ang paglusaw ng asin ay hindi isang kemikal na reaksyon, ngunit phase transition
Ano ang kapasidad ng init kumpara sa tiyak na init?

Ang kapasidad ng init ng molar ay isang sukatan ng dami ng init na kinakailangan upang mapataas ang temperatura ng isang mole ng isang purong sangkap ng isang degree K. Ang tiyak na kapasidad ng init ay isang sukat ng dami ng init na kinakailangan upang itaas ang temperatura ng isang gramo ng isang purong sangkap sa pamamagitan ng isang degree K
