
- May -akda Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Huling binago 2025-01-22 17:12.
Mula sa itaas hanggang ibaba pababa a pangkat , bumababa ang electronegativity. Ito ay dahil ang atomic bumababa ang bilang a pangkat , at sa gayon ay may tumaas na distansya sa pagitan ng mga valence electron at nucleus, o mas malaki atomic radius.
Kung isasaalang-alang ito, bakit tumataas ang laki ng atomic sa isang grupo?
Sa pangkalahatan, atomic radius bumababa sa isang panahon at tumataas pababa sa isang grupo . Pababa ng isang grupo , ang bilang ng mga antas ng enerhiya (n) nadadagdagan , kaya ayan ay isang mas malaking distansya sa pagitan ng nucleus at ang pinakalabas na orbital. Nagreresulta ito sa isang mas malaki atomic radius.
Gayundin, ano ang trend sa 1st ionization energy mula sa itaas hanggang sa ibaba pababa ng isang grupo? Gumagalaw pakaliwa pakanan sa isang yugto, atomic radius bumababa, kaya ang mga electron ay mas naaakit sa (mas malapit) nucleus. Ang pangkalahatang trend ay para sa enerhiya ng ionization upang mabawasan ang paglipat mula sa itaas hanggang sa ibaba pababa sa isang pangkat ng periodic table. Ang paglipat pababa sa isang grupo, isang valence shell ay idinagdag.
Alamin din, ano ang pana-panahong kalakaran sa pagkakaiba-iba ng Valency habang bumababa sa isang grupo?
» Lahat ng miyembro ng a pangkat may parehong bilang ng mga valence electron. » Ang atomic radius ay karaniwang tumataas habang pababa ng isang grupo dahil sa pagdaragdag ng isang bagong antas ng enerhiya (shell).
Anong trend sa atomic radius ang nakikita mo habang bumababa ka sa isang grupong pamilya sa periodic table?
Ang isang mas malakas na pack ng nucleus ay humihila ng mga electron palapit, pinagsasama ang mga ito nang mas mahigpit at, sa huli, binabawasan ang atomic radius . Bilang bumaba ka a pamilya sa periodic table , bumababa ang enerhiya ng ionization. Ang bilang ng mga antas ng enerhiya ay tumataas habang bumaba ka ang periodic table.
Inirerekumendang:
Ano ang tamang pagkakasunod-sunod ng mga layer ng atmospera ng lupa mula sa ibaba hanggang sa itaas?

Ano ang tamang pagkakasunod-sunod ng mga layer ng atmospera ng lupa mula sa ibaba hanggang sa itaas? Stratosphere, Mesosphere, Troposphere, Thermosphere, Exosphere
Ano ang unang hakbang sa pagbuo ng isang patayo mula sa isang punto hanggang sa isang linya?
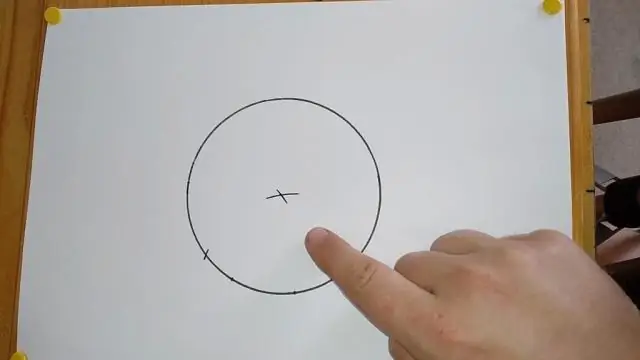
Ikonekta ang ibinigay na punto sa punto kung saan nagsa-intersect ang mga arko. Gumamit ng isang tuwid na gilid upang matiyak na ang linya ay tuwid. Ang linya na iyong iginuhit ay patayo sa unang linya, sa pamamagitan ng ibinigay na punto sa linya
Ano ang tamang pagkakasunod-sunod ng mga atmospheric layer ng Earth mula sa ibaba hanggang sa itaas?

Troposphere, Stratosphere, Mesosphere, Thermosphere, Exosphere. (Ito ay mula sa ibaba hanggang sa itaas.)
Paano gumagana ang prinsipyo ng Aufbau na kung ano ang ibig sabihin ng sabihin na ang mga orbital ay pinupuno mula sa ibaba pataas o itaas pababa depende sa diagram)?

Mula sa Ibaba Pataas: Dapat punan ang mga silid mula sa ground floor pataas. Sa mas matataas na palapag, maaaring magbago ng kaunti ang pagkakasunud-sunod. Prinsipyo ng Aufbau: pinupuno ng mga electron ang magagamit na mga orbital mula sa pinakamababang enerhiya hanggang sa pinakamataas na enerhiya. Sa ground state lahat ng mga electron ay nasa pinakamababang posibleng antas ng enerhiya
Ano ang tamang pagkakasunod-sunod ng mga layer ng atmospera mula sa ibaba hanggang sa itaas?

Ano ang tamang pagkakasunod-sunod ng mga layer ng atmospera ng lupa mula sa ibaba hanggang sa itaas? Stratosphere, Mesosphere, Troposphere, Thermosphere, Exosphere
