
- May -akda Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Huling binago 2025-01-22 17:12.
Reaksyon Ang mga intermediate ay nabuo sa isa hakbang at pagkatapos ay natupok sa ibang pagkakataon hakbang ng mekanismo ng reaksyon . Ang pinakamabagal na hakbang nasa mekanismo ay tinatawag na ang pagtukoy ng rate o naglilimita sa rate hakbang . Ang pangkalahatang reaksyon ang rate ay tinutukoy ng mga rate ng hakbang hanggang sa (at kasama) ang hakbang sa pagtukoy ng rate.
Ang dapat ding malaman ay, paano mo mahahanap ang pinakamabagal na hakbang sa isang reaksyon?
Ang rate pagtukoy ng hakbang ay ang pinakamabagal na hakbang ng isang kemikal reaksyon na tumutukoy sa bilis (rate) kung saan ang pangkalahatang reaksyon nalikom.
Sagot
- Ang hakbang sa pagtukoy ng rate ay ang pangalawang hakbang dahil ito ang mabagal na hakbang.
- 2NO+2H2→N2+2H2O.
- Ang mga intermediate sa reaksyong ito ay N2O2 at N2O.
Bukod pa rito, ano ang reaksyon ng unang order? A una - utos ng reaksyon ay isang reaksyon na nagpapatuloy sa isang rate na nakadepende nang linear sa isang reactant concentration lamang.
Ang dapat ding malaman ay, bakit ang hakbang sa pagtukoy ng rate ay ang pinakamabagal na hakbang sa isang mekanismo ng reaksyon?
Ang rate - ang pagtukoy ng hakbang ay ang pinakamabagal na hakbang sa isang mekanismo ng reaksyon . Dahil ito ay ang pinakamabagal , tinutukoy nito ang rate ng pangkalahatang reaksyon . Ito ay i-explore sa ibang pagkakataon nang mas detalyado. Pagbabago sa konsentrasyon ng mga kemikal sa paglipas ng panahon: Isang plot ng oras kumpara sa konsentrasyon para sa dalawang species sa chemical equilibrium.
Paano mo mahahanap ang pangkalahatang reaksyon?
Ang pangkalahatang reaksyon ang rate ay tinutukoy ng mga rate ng mga hakbang hanggang sa (at kasama) ang pinakamabagal na elementarya na hakbang. Ang pinakamabagal na hakbang sa a reaksyon Ang mekanismo ay tinatawag na rate determining o rate limiting step. Para sa aming halimbawang mekanismo sa nakaraang seksyon, ang hakbang sa paglilimita sa rate ay ang unang hakbang sa elementarya.
Inirerekumendang:
Ano ang epekto ng isang katalista sa mekanismo ng isang reaksyon?

Ang isang katalista ay nagpapabilis ng isang kemikal na reaksyon, nang hindi natupok ng reaksyon. Pinapataas nito ang rate ng reaksyon sa pamamagitan ng pagpapababa ng activation energy para sa isang reaksyon
Ano ang elementarya na hakbang sa mekanismo ng reaksyon?

Ang elementarya na hakbang (o elementarya na reaksyon) ay isang hakbang sa isang serye ng mga simpleng reaksyon na nagpapakita ng pag-unlad ng isang reaksyon sa antas ng molekular. Ang mekanismo ng reaksyon ay ang pagkakasunud-sunod ng mga elementarya na hakbang na magkakasamang bumubuo ng isang buong kemikal na reaksyon
Paano mo mahahanap ang equation ng isang linya na binigyan ng isang punto at isang parallel na linya?
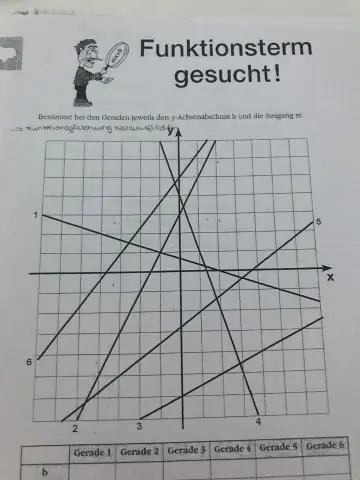
Ang equation ng linya sa theslope-intercept form ay y=2x+5. Ang slope ng parallelline ay pareho: m=2. Kaya, ang equation ng parallel na linya ay y=2x+a. Upang makahanap ng a, ginagamit namin ang katotohanan na ang linya ay dapat dumaan sa ibinigay na punto:5=(2)⋅(−3)+a
Paano mo i-graph ang isang equation nang hakbang-hakbang?
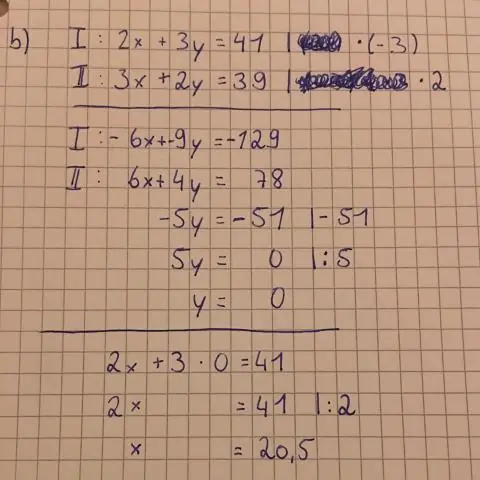
Narito ang ilang hakbang na dapat sundin: Isaksak ang x = 0 sa equation at lutasin ang y. I-plot ang punto (0,y) sa y-axis. Isaksak ang y = 0 sa equation at lutasin ang x. I-plot ang punto (x,0) sa x-axis. Gumuhit ng isang tuwid na linya sa pagitan ng dalawang puntos
Paano ka gumawa ng isang slope nang hakbang-hakbang?

May tatlong hakbang sa pagkalkula ng slope ng isang tuwid na linya kapag hindi ka binigyan ng equation nito. Unang Hakbang: Tukuyin ang dalawang punto sa linya. Ikalawang Hakbang: Piliin ang isa para maging (x1, y1) at ang isa ay magiging (x2, y2). Ikatlong Hakbang: Gamitin ang slope equation upang kalkulahin ang slope
